Todas las preguntas relativas a la utilización de Flashkits
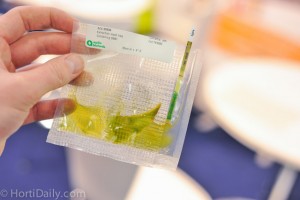
¿Por qué no aparece la línea de control? ¿Por qué la intensidad de la línea de control es débil?
La ausencia o muy baja intensidad de la línea de control significa que el resultado de la prueba no es válida. Este resultado puede explicarse por el hecho de que la tira ha sido buceo demasiado profundamente en la bolsa de extracción que contiene la muestra. La cinta no debe estar demasiado sumergido en el jugo de extracción. Debe ser insertado hasta la línea blanca debajo de las flechas presentes en la parte de color de la tira.
Las otras causas posibles, que siguen siendo muy raros, son los siguientes:
• La prueba no es compatible con la muestra,
• El Flashkit no se ha almacenado correctamente de acuerdo con las condiciones especificadas,
• Ha pasado la fecha de vencimiento de la prueba.Por mas información no dude en contacto con nosotros.
¿Por qué mi resultado de la prueba aparece débilmente?
¿Lo que es La línea de control es más oscuro y claramente visible desde la línea de prueba?Si este no es el caso, la prueba puede ser considerada válida. Varios factores pueden explicar este resultado, que un mal almacenamiento o demasiado profunda inmersión de la tira en la muestra. Si la línea de control es visible y válida, y se ve un resultado ligeramente positivo, esto se explica por una baja concentración de la muestra patógeno. El resultado puede aparecer bajo debido a la presencia del patógeno objetivo a baja concentración se aproxima al límite de detección de prueba. Para validar este resultado, se puede realizar una nueva prueba de una muestra fresca con síntomas. La mayoría de las pruebas Flashkits pueden detectar con fiabilidad las muestras y los agentes patógenos nuevos casos de infección en bajas concentraciones. Para obtener más información, póngase en contacto con nosotros.
Salí de mi tubo de Flashkits fuera del refrigerador durante la noche, mi prueba es utilizable?
Los tubos se proporcionan en los tubos que contienen ensillados desecante, por consiguiente, deben funcionar correctamente. Todo se someten a pruebas de estabilidad tira rigurosos que también proporcionan una buena resistencia durante las entregas durante varios días.
Sin embargo, si el tubo se dejó abierta durante mucho tiempo en un lugar húmedo, hay una buena probabilidad de que las cintas han absorbido la humedad, y por lo tanto no pueden ser utilizados dentro de los estándares de calidad requeridos. Siempre asegúrese de dejar la fresca tubo cerrado (+ 4/6 ° C) cuando no esté usando pruebas.
¿Hasta qué punto mis resultados fiables?
Agdia pone un punto de honor para desarrollar Flashkits pruebas que son tan sensibles y precisos que equivalente al formato de ELISA, donde esté disponible. De hecho, las tiras reactivas pueden alcanzar los mismos niveles de fiabilidad y confianza, mientras que el ahorro de tiempo mediante el uso de las Flashkits lugar ELISA.
Durante el desarrollo de nuestras tiras de prueba, buscamos la mayor cantidad de analitos y los posibles cambios para asegurar un alto nivel de precisión. Indicamos la guía del usuario hallazgos reacciones no específicas con ciertos tipos de muestras o analitos.
Nuestros Flashkits están garantizados por un año desde la fecha de compra si han sido debidamente mantenido en las condiciones indicadas en el envase.
¿Hay una línea verde en lugar de la línea de prueba, lo que es debido y cómo se interpretan los resultados?
Muy a menudo, las líneas verdes son causadas por una muestra demasiado concentrada. Para resolver el problema, puede realizar las diluciones de la muestra con el tampón apropiado o preparar una nueva muestra con menos tejido de la planta.
Si no se puede repetir la prueba con uno de estos dos métodos, se puede concluir que la prueba es negativa si no se percibe el color rojo o púrpura. Sin embargo, se recomienda encarecidamente para volver a probar, porque la línea verde puede ocultar potencialmente una baja concentración del patógeno.
¿Al final de la prueba, interpreto la prueba negativa. Ahora que la prueba está seco, puedo ver una línea¿Qué significa ?
En la mayoría de los casos esta anomalía aparece cuando la tira se mantiene en contacto con la muestra pasado el tiempo especificado en el protocolo. Si la tira no se retira a tiempo el líquido continúa migrando a lo largo de la tira, causando un ligero falso positivo. En este caso, le recomendamos que pruebe de nuevo la muestra mediante la eliminación de la tira en el tiempo especificado en las instrucciones.
Todas las respuestas a sus preguntas sobre el ELISA

¿Por qué mi ELISA no produce colores?
Comprobar estos valores con cuidado, pueden explicar el problema:
• Es posible que no haya añadido el conjugado enzimático
• VQue utilizó el anticuerpo de captura en lugar de la enzima conjugada
• El control positivo puede estar inactivo
• Es posible que haya olvidado de añadir la tableta deel tampón sustrato PNP con el sustrato PNP
¿Puedo mantener mi plato después de haber coatées?
Todas las placas Agdia se pueden almacenar durante largos periodos si postcoated con el tampón postrecubrimiento apropiado. Póngase en contacto con nosotros directamente para obtener más información.
¿Por qué apareció el color en todas mis pozos de la placa?
Es posible que no haya limpiado su plato correctamente
El sustrato puede haber sido contaminado. PNP tabletas pueden haber sido contaminados por tocar
El sustrato o placa potencialmente han estado expuestos a la luz brillante
Es posible que haya puesto las muestras positivas en todos los pozos
Que utilizó un tampón de edad que ha sido contaminada con el tiempo
Usted Coate la placa con la enzima conjugado o con recubrimiento de anticuerpos contaminados con la enzima conjugada. Utilice siempre nueva pipeta estéril con conos.
¿Por qué el color apareció en todos los pozos que están en el borde de la placa?
Usted no puede haber lavado los extremos correctamente
Las placas de mala calidad pueden causar esto. Lo cual no puede decirse de las nuevas placas de ELISA de alta calidad, tales como los proporcionados por Agdia-Emea.
¿Por qué un color aparece inesperadamente en los pozos que están alrededor de las muestras positivas o controles positivos?
Probablemente contaminado los pozos circundantes durante la etapa de lavado. Para ver cómo lavar una placa de ELISA, miranuestros vídeos de demostración.
¿Por qué recibo lo que parece ser falsos positivos con mis muestras?
La muestra de la planta evaluados es realmente positivo
Sus muestras pueden estar contaminados a través de su equipo de molienda de la muestra
¿Por qué mis positivos son débiles?
• Sus componentes del kit han pasado la fecha de vencimiento
• La pruebas o análisis patógeno está presente en cantidades demasiado pequeñas para ser detectadas
• Que utilizó un tampón de extracción apropiado
• (Para las pruebas de fosfatasa alcalina) de haber preparado el tampón PBST PNP usando en lugar de agua destilada. El contenido de fosfato en tampón PBST puede reducir la intensidad del color generado.
• Usted ha demasiado diluida el conjugado enzima o el substrato.
¿Por qué mis componentes de la prueba tienen olor a descomposición?
Los componentes deben estar contaminados y no deben usarlos.
¿Cuánto tiempo podemos hacer un prueba ELISA?
Agdia-ELISA protocolos ofrecen el más flexible y seguro como sea posible. Nuestros kits Pathoscreen se pueden hacer dentro de 5 horas (con incubación de la muestra durante 2 horas o durante la noche, combinado sustrato 2h,y substrato 1H). Los reactivos permiten a realizar las pruebas en 6-8 horas (recubrimiento durante 4 horas o toda la noche, la muestra 2 horas o toda la noche).
¿Cuáles son las temperaturas ideales para mantener los reactivos y para la realización de la prueba?
Los productos Agdia-Emea se han desarrollado para ser altamente sensibles y específicos mientras que ser lo suficientemente robusta como para soportar variaciones de temperatura y fases sin refrigeración durante el parto. Las temperaturas de incubación y almacenamiento que aparecen en nuestros productos y guías de usuario reflejan condiciones medias observadas en nuestros laboratorios. Para asegurarse de que su examen se puede realizar de manera óptima, se recomienda mantener los componentes en un refrigerador entre 2 y 8 ° C.
Al realizar la prueba o mantener los componentes a temperatura ambiente, se recomienda hacer entre -3 ° C y + 21 ° C. En la mayoría de los casos, los cambios en las temperaturas fuera de estos límites no afectarán de manera significativa el resultado de la prueba cualitativa, sin embargo, Agdia-Emea no puede garantizar la realización de la prueba en los límites de temperatura descritos anteriormente. Entendemos que las temperaturas en su área pueden ser diferentes de nuestros laboratorios de validación, por lo que si usted tiene alguna pregunta sobre sus condiciones locales, por favor, póngase en contacto con nosotros.
Todas las preguntas sobre AmplifyRP®

¿Cuáles son las ventajas que ofrece el AmplifyRP® en comparación con la PCR tradicional en tiempo real ?
PCR es una prueba de ADN altamente sensible y específico, sin embargo, requiere de habilidades especiales y sólo se puede conseguir en el laboratorio. La mayoría de los análisis de PCR en primer lugar requiere una etapa de purificación del ADN. Para este paso, utilizar kits de purificación muy caros y reactivos a veces tóxicos. PCR también requiere la repetición de las reacciones a diferentes temperaturas de acuerdo con un ciclo específico facilitado por termocicladores. Pero este ciclo de calor sigue siendo un paso muy largo. En conclusión, la aplicación de PCR de un equipo costoso, habilidades técnicas y muchas horas de manipulaciones.
AmplifyRP® es una plataforma de pruebas de ADN y ARN igual de sensible y específica que la PCR pero no requieren la compra de un equipo costoso y se puede hacer por los usuarios de todos los niveles, y esto sólo en alrededor de 30 minutos :
• El coste total para el equipo es 315€
• El análisis se puede realizar en muestras crudas
• El tiempo de ejecución de la prueba es de entre 25 y 40 minutos, incluyendo el tiempo de preparación de muestras
• El formato es fácil de usar y fácilmente transportable.
¿Es necesario un entrenamiento especial para usar Amplifier®?
No, Amplify fue creado para cualquier tipo de usuario final. Todos los reactivos e instrumentos desechables necesarios para el análisis se incluyen en el kit. Otros equipos se pueden pedir con antelación por un paquete de inicio.
AmplifyRP® Los kits están diseñados para limitar el número de pasos en el protocolo. Todos los reactivos de amplificación son liofilizadas en tubos de un solo uso. La única manipulación que el usuario debe realizar es rehidratar el reactivo e inserte la muestra. Dado que se lleva a cabo este paso, la amplificación y la detección se puede hacer entre 15 y 30 minutos, dependiendo del formato.
¿Qué parte de mi muestra mixta debo usar para la prueba?
Utilizando un asa estéril, se recoge una muestra de la solución de extracción de la muestra que está completamente mezclado. No añada trozos de tejido para el medio reactiva.
¿Qué pasará si añado más 1 µl por reacción?
La cantidad de extracción de la muestra que se añade es de aproximadamente 1 ul. Ligeros cambios en el volumen agregado (1 µl o menos) no afectan al rendimiento de pruebas.
¿Puedo usar un tampón de extracción que no sea la recomendada para la prueba?
No, sólo el tampón de extracción suministrada con el kit está validado para la prueba. Moler el tejido en cualquier otro tampón puede conducir a resultados negativos falsos.
¿Qué pasará si se incubó la reacción a una temperatura más alta de lo esperado?
Si usted anima la reacción a temperaturas significativamente más alta que 39°C (42°C o más), las enzimas serán inactivada que aumenta la probabilidad de resultados negativos falsos.
¿Qué pasará si se incubó la reacción a una temperatura más baja de lo esperado?
Si usted anima a su reacción a una temperatura inferior a 39 ° C, la reacción será más lenta. Mientras que una temperatura de incubación más baja requiere un tiempo de incubación más largo, agregue la respuesta a la cámara de detección demasiado pronto puede llevar a resultados negativos falsos.
¿Qué sucederá si la etapa de calentamiento se interrumpe?
Si su unidad de calefacción se detiene durante la reacción o si usted mezcló la muestra en el tubo de reactivo sin un calentador de inmediato, la prueba puede seguir siendo válida. Cuando note que la unidad de calefacción ha fallado o se ha desconectado inadvertidamente, sustituya los tubos de la fuente de calor durante 15 minutos adicionales, a continuación, siga las instrucciones recomendadas.
¿Tiene un protocolo de insectos u otros tejidos?
Si un protocolo de extracción para un tipo particular de tejido no se describe en nuestras guías de usuario, entre en contacto con nosotros por correo electrónico info@agdia-emea.com o teléfono +33 (0) 1 60 78 81 64.
¿Puedo quitar la tira a la cámara de detección para mis archivos?
Después de cerrar la cinta, no intente volver a abrirlo. Abrir o dañar el casete después del final de la reacción puede causar la contaminación de la zona de trabajo y resultados falsos positivos. Si desea mantener un registro de sus resultados, se recomienda hacer una fotografía de la tira.
¿Qué debo hacer si la tapa de mi tubo de reacción se abre antes de fijar en la cámara de detección?
Tras el final de la reacción, si se abre el microtubo antes de que quede fijado en la cámara de detección, tomar el examen y limpiar el área. Si usted cree que ha expuesto su área de trabajo al contenido de microtubo tras el final de la reacción, lavarse las manos y limpiar las superficies circundantes con cloro antes de realizar otra prueba.
¿Cómo lanzo el dispositivo una vez que se haya completado la prueba?
La cámara de detección y el equipo asociado pueden ser desechadas con la basura normal. No abrir o desmontar el cassette.
¿Esta prueba contiene un control de amplificación como algunas reacciones de PCR?
No. La línea de control en una prueba Acceler8 es una medida del rendimiento de la migración de la banda, no el rendimiento de la extracción de ácidos nucleicos. Testigo de amplificación interna de dicho amplificar genes “limpieza” se utilizan en reacciones de PCR para detectar la presencia del ácido nucleico del huésped (planta) después de la purificación de ácidos nucleicos. La tecnología AmplifyRP® utiliza extractos de plantas crudos y no requiere de purificación que puede conducir a la pérdida de ADN o ARN, lo que no hay necesidad de un control interno de amplificación.
¿Qué debo hacer si el producto parece estar dañado?
Póngase en contacto con Agdia Biofords inmediatamente si nota un defecto en envases o componentes del kit o se olvida un elemento en su pedido.
¿A quién puedo contactar si tengo preguntas sobre el rendimiento de la prueba?
Gracias a ponerse en contacto por email info@agdia-emea.com o por téléfono +33 (0) 1 60 78 81 64.






